Реакция термического разложения арсина
Содержание:
- Мышьяка гидрид
- Клиническая информация, средства защиты, первоочередные действия в очаге
- АРСИНЕ: число взаимодействия с миром «6»
- номенклатура
- Дифенилхлорарсин
- АРСИНЕ: число истинных особенностей «7»
- приложений
- Токсические эффекты
- Физико-химическая характеристика
- Химические свойства
- Структура арсина
- АРСИНЕ: число душевных стремлений «8»
- Токсичность и опасность
Мышьяка гидрид
Определение гидрида мышьяка. Газоанализатор регистрирует концентрацию АэНз до 5 мг/м3, минимальная определяемая концентрация 0,15 мг/м3. Точность определения ± 10%. При повышении концентрации АэН3 до 1,5 мг/м3 подается предупредительный световой сигнал, а при концентрации 3 мг/м3 — аварийный звуковой сигнал.
Определению мешают гидриды мышьяка сурьмы и олова, кремний.
Очень опасные соединения мышьяка — As(3+), As(5+), монометил- и ди-метиларсенаты — определяли после экстракции и дериватизации контролируемых компонентов в загрязненной речной воде, в которую поступали с/х и промышленные сточные воды . Полученный экстракт анализируют методом ГХ/ПИД на капиллярной колонке (10 м х 0,53 мм) с силиконовой НЖФ. Содержащиеся в этихже пробах неорганические соединения мышьяка определяют методом ААС после генерации летучих гидридов (см. выше).
Определению германия не мешают мышьяк, сурьма, олово, кремний. Определению гидрида германия мешают гидриды мышьяка, сурьмы и олова.
Легко окисляется и гидролизуется в воздухе большинство гидридов. Из летучих гидридов сравнительно медленно разлагаются водой лишь гидриды, германия, олова, фосфора, мышьяка и сурьмы. Особенно неустойчивы и чрезвычайно легко разлагаются влагой воздуха бороводороды. Сложные превращения претерпевают во влажном воздухе оксиды азота, а также многие галогены и их производные, которые как и все агрессивные соединения, могут кроме того взаимодействовать между собой и с присутствующими в воздухе неорганическими и органическими соединениями. Чрезвычайно реакционноспособно большинство металлорганических соединений, разлагающихся кислородом и влагой воздуха .
Сущность метода заключается в атомно-абсорбционном определении мышьяка, полученного термическим разложением гидрида мышьяка. Гидрид мышьяка получают при взаимодействии тетрагидробората натрия с мышьяком.
Во-вторых, при восстановлении боргидридом натрия образуются п образные гидриды мышьяка, сурьмы, висмута и селена, способные дезак вировать поверхность золотого сорбента . Влияние селена определение ртути зависит от его валентности: селен (VI) практическр влияет на аналитический сигнал ртути, а селен (IV) существенно его уме шает. Если используется жесткое окисление с использованием перманганата персульфата калия в присутствии азотной или серной кислот, селен окисляется до селена (VI), поэтому его мешающее влияние не проявляе Если такое окисление проб не предусмотрено, то уменьшение сигнала жет достигать 30; 63 и 77 % при 333-, 1667- и 3333-кратном превыше концентраций селена над содержанием ртути.
Индикаторную ленту готовят из чертежной бумаги. Полосу бумаги пропитывают в течение одних суток 5% спиртовым раствором бромида ртути. В присутствии гидрида мышьяка индикаторная бумага окрашивается в желтовато-коричневый цвет. Расход индикаторной ленты — 9 м в сутки.
Уаэак.ЗесЦуес рекомендуют метод определения мышьяковистого, фосфористого и сурьмянистого водорода в воздухе, основанный на образовании окрашенных соединений при взаимодействии гидридов мышьяка, фосфора и сурьмы с пиридиновым раствором диэтилдитиокарбамата серебра.
Особенно эффективной для экологических анализов является мультианалитическая система (комплексная спектральная аналитическая лаборатория), включающая несколько аналитических приборов (фирма Хьюлетт-Паккард, 1999 г.), управляемых компьютером. Схема одного из таких комплексов изображена на рис. 111.37.
Для превращения растворов анализируемых веществ в атомный пар чаще всего применяют щелевые горелки длиной 5-10 см. Они довольно однотипны по конструкции и легко заменяются. Большинство приборов рассчитаны на использование в качестве окислителей воздуха, кислорода и закиси азота, а в качестве топлива — пропана, ацетилена и водорода Наибольшее распространение получило воздушно-ацетиленовое пламя (2200-2400 °С), которое позволяет определять многие высокотоксичные металлы (РЬ, Сс1, Zn, Си, Сг и др.). Для определения элементов с более высокой температурой парообразования (А1, Ве, Мо и др.) широкое признание получила смесь закись азота-ацетилен (3100-3200 °С), поскольку она более безопасна в работе, чем смеси с кислородом. Для обнаружения мышьяка и селена в виде гидридов требуется восстановительное пламя, образующееся при сжигании водорода в смеси аргон-воздух.
Клиническая информация, средства защиты, первоочередные действия в очаге
| Общий характер действия |
|
| Средства защиты | Для химразведки и руководителя работ — ПДУ-3 (в течение 20 минут). Для аварийных бригад — изолирующие противогаз ИП-4М и спецодежда. При возгорании — огнезащитный костюм в комплекте с самоспасателем СПИ-20. |
| Химический очаг | |
| Вид очага | Нестойкий, замедленного действия. Пары скапливаются в нижних этажах зданий, подвалах, низинах, оврагах. |
| Первоочередные мероприятия | Проведение поисково-спасательных работ в очаге, в том числе оказание первой медицинской помощи пострадавшим и их вынос (вывоз) на временные пункты сбора в оптимальные для спасения жизни и сохранения здоровья сроки, ведение разведки, обозначение и оцепление очага. Изолировать опасную зону в радиусе не менее 200 м. Откорректировать указанное расстояние по результатам химразведки. Держаться наветренной стороны. Избегать низких мест. Соблюдать меры пожарной безопасности. В опасную зону входить в защитных средствах. Приинтенсивной утечке дать газу полностью выйти. Изолировать район, пока газ не рассеется. Не приближаться к емкостям. Не прекращать горения при наличии утечки. Тушить тонкораспыленной водой, пеной, порошками с максимального расстояния. Охлаждать емкости водой с максимального расстояния. Пары осаждать тонкораспыленной водой. |
АРСИНЕ: число взаимодействия с миром «6»
«Шестерочника» легко узнать – это тот самый человек, который отличается необыкновенной удачливостью, всегда окружен друзьями, имеет прекрасную семью и не понаслышке знает, что такое взаимная любовь. Баловень судьбы? На самом деле это не совсем так. Все, что получает «шестерочник» с кажущейся легкостью, им заслужено. Этот человек отличается спокойным, уравновешенным характером, умением помочь в трудной ситуации, дать толковый совет или просто выслушать того, кому необходима моральная поддержка. В служении другим на самых разных уровнях люди шестерки часто находят смысл своей жизни; именно они умеют отдавать, ничего не теряя, и спокойно принимать любые дары. Близкие и друзья «шестерочника» чувствуют себя рядом с ним спокойно и комфортно – такой человек не играет в психологические игры, не пытается ими манипулировать, говорит именно то, что думает, но в форме, которая никого не обидит.
«Шестерочник» — отличный семьянин, причем его заботят не только уют дома и успешность всех членов семьи, но и душевное состояние близких. Это несравненный хранитель домашнего очага, умный и терпеливый наставник, достойный пример для подражания. Заботясь об окружающих, люди шестерки часто забывают о себе, и один из важных уроков, которые им следует усвоить – не растрачивать себя без остатка, поскольку силы их велики, но все же не неисчерпаемы.
Стремление «шестерочников» к гармонии накладывает отпечаток не только на их отношения с людьми, но и на то, как они организовывают свою жизнь – от основополагающих тенденций, до мелочей. Можно не сомневаться, что квартира человека шестерки чиста и уютна, рабочее место – комфортно и располагает к продуктивному труду, а место отдыха радует глаз приятным пейзажем. «Шестерочники» не только ценят красоту, но и способны увидеть ее во всем, что их окружает
Именно поэтому они часто обладают незаурядными талантами в области дизайна, и, что немаловажно, способны помочь любому раскрыть лучшие стороны своей души
Если «шестерочникам» что и мешает в жизни, так это неспособность принять решение быстро, и не отступать от него ни на шаг. Такие люди способны помогать другим, давать простые и разумные советы, но сами часто терзаются беспричинными сомнениями, нервничают и переживают по мелочам. Они восприимчивы к радостям жизни, но и беды принимают близко к сердцу; часто реагируют излишне эмоционально и подолгу страдают от душевных ран.
номенклатура
В предыдущем разделе были упомянуты другие имена, принятые для арсина. Учитывая, что это бинарный гидрид между мышьяком и водородом, его можно назвать по систематической, стандартной и традиционной номенклатуре..
В систематической номенклатуре подсчитайте количество атомов водорода. Таким образом, его название становится: тригидрид мышьяка.
Его название в соответствии с номенклатурой запаса очень похоже, но добавляя его нагрузку с римскими цифрами в скобках: гидрид мышьяка (III),.
Что касается традиционной номенклатуры, ее название арсин или арсано.
Его также можно назвать арсенидом водорода; однако это не совсем правильно, поскольку подразумевает, что мышьяк является более электроотрицательным, чем водород, и участвует в связи как As3-.
Дифенилхлорарсин
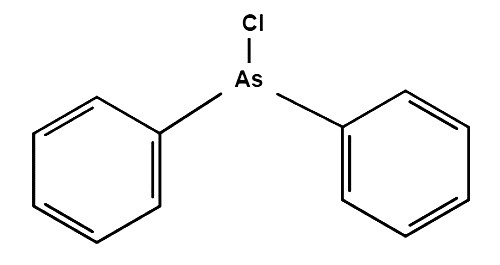 Структурная формула дифенилхлорарсина
Структурная формула дифенилхлорарсина
Газ арсин дифенилхлорарсин (формула — (C6H5)2AsCl) по американской номенклатуре обозначается как «Д.А.», а по немецкой «Blaukreuzstoff-Clark I». Дает сильное раздражающее действие, относится к разряду чихательных боевых отравляющих веществ. Как и предыдущий арсин дает усиление действия, даже по выходе из отравленной зоны.
Под влиянием паров газа арсина через несколько часов на коже может появиться эритема, сопровождаемая ощущением жжения и зуда. При непосредственном воздействии на кожу образуются пузыри и даже очаги омертвения. При действии через кожу газа дифенилхлорарсина возможны явления общего отравления в виде гиперестезий, анестезией и парестезий.
Оба упомянутых в данной медицинской статье газооборазных арсина, как боевые отравляющие вещества, не предполагают воздействия на кожу. Они находят себе боевое применение в виде дымов, и раздражение кожи может возникнуть случайно.
Первая помощь при отравлении
Так как, с точки зрения опасности для жизни, поражения этилдихлорарсином и дифенилхлорарсином далеко не столь значимы, как от иприта и люизита, то главнейшие мероприятия идут в сторону воздействия на дыхательные пути. По Walton и Eldridge, вдыхание хлора представляет собой дающее хороший эффект средство при этих отравлениях (концентрация 0,015-0,019 мг на литр). Небольшие кожные поражения в виде эритемы, а редко и раздражение слизистых оболочек через 1—2 дня проходят; даже при наличии общих явлений отравления арсинами прогноз остается благоприятным.
АРСИНЕ: число истинных особенностей «7»
Люди, которые находятся под воздействием цифры 7, воспринимают окружающую действительность спокойно и умиротворенно. Они всегда подчиняются голосу разума и имеют завидное самообладание. Когда находящиеся возле них теряют самоконтроль – люди семерки остаются полностью спокойны, и берут ситуацию в свои руки.
При пожаре «семерочник» первым вспомнит о плане эвакуации, а при кораблекрушении разыщет спасательные жилеты и шлюпки. Он не боится экспериментировать, убедившись вначале, что не повредит этим себе и своему окружению.
В пиковых ситуациях «человек-семерка» необходим, но и в повседневной жизни его сообразительность уж точно не помешает. «Семерочник» удовлетворен своей жизнью. Он не ставит перед собой невыполнимых задач и не жалеет о случившемся, всегда поступает обдуманно, но не чужд разумного риска. Он упускает из виду мелочи, что иногда сильно его подводит. Однако, поставив перед собой цель, человек семерки, обычно, ее достигает, благодаря поддержке надежных соратников.
«Семерочник» способен отстоять свои интересы, но и об окружающих не забывает. Он прилагает максимум усилий, чтобы улучшить жизнь близких, но его волнуют и глобальные проблемы, в решении которых он участвует по мере своих сил. Человек семерки не пройдет мимо чужих страданий, из-за обостренного чувства справедливости и умения сопереживать незаслуженно обиженным.
Обычно эти люди выбирают независимую деятельность. При работе в коллективе, они затрачивают слишком большое количество сил, для установления комфортной, спокойной, товарищеской обстановки среди коллег. «Семерочник» предпочитает не использовать проторенные пути.
Для него интересно добиться успеха на той стезе, где других постигла неудача. Таким образом, он показывает себе и всем остальным, что для него, как для человека, сильно увлеченного какой-либо идеей, все в этом мире возможно.
приложений
Полупроводниковые материалы
Арсин используется в производстве полупроводниковых материалов, с использованием в микроэлектронике и твердотельных лазерах. Он используется в качестве легирующей добавки кремния и германия. Арсин используется в производстве GaAs полупроводника.
Используемая процедура представляет собой химическое осаждение из паровой фазы (ХОПФ) при 700 — 900 ºC в соответствии со следующей реакцией:
Ga (CH3)3 + AsH3 => GaAs + 3CH4
Химическое вооружение
Арсин — смертельный газ, поэтому думали об его использовании в химической войне. Но он никогда официально не использовался в качестве химического оружия из-за его высокой воспламеняемости и более низкой эффективности по сравнению с другими менее легковоспламеняющимися соединениями.
Тем не менее, некоторые органические соединения, полученные из арсина, многие более стабильные, показали, что они применимы в химической войне, например, люизит (β-хлорвинил дихлоарсин).
лиганды
Арсин — это газ, который воспламеняется в воздухе, но его органические производные обладают большей стабильностью, например, AsR.3 (R = алкильные или арильные группы), используются в качестве связующих в координационной химии металлов.
Как (С6H5) является мягким связующим и, следовательно, обычно включается в комплексы металлов, которые имеют центральные атомы с низким уровнем окисления (мягкие катионы).
Токсические эффекты
Его токсичность такова, что при концентрации в воздухе 250 ч / млн мгновенно смертелен. Может быть смертельным при 30-минутном воздействии при концентрации вдыхаемого воздуха 25-50 промилле.
Большая часть токсического действия арсина производится при вдыхании. Он способен пересекать альвеолярную стенку и попадать в кровь, где оказывает токсическое действие, которое воздействует на эритроциты и функцию почек..
Отравление арсином проявляется появлением нарушений сознания, шока, гематурии, желтухи и почечной недостаточности.
Действие на эритроциты и гемоглобин
Арсин оказывает несколько воздействий на стенку эритроцитов и гемоглобин. Это способствует освобождению гемовой группы от гемоглобина. Арсин является непрямым гемолитическим агентом, действует, подавляя действие каталазы.
Это приводит к накоплению перекиси водорода (Н2О2), что вызывает разрыв мембраны эритроцитов. С другой стороны, арсин вызывает снижение внутриклеточной концентрации восстановленного глутатиона (GSH), что способствует разрушению мембраны эритроцитов.
Массивный гемолиз является летальным и проявляется снижением концентрации гемоглобина и гематокрита в крови; увеличение сывороточной концентрации гемоглобина и билирубина; и гематурия.
Почечная недостаточность является следствием осаждения гемоглобина в виде цилиндров в почечных канальцах, наблюдаемого при вскрытии. Хотя в лабораторных условиях также было обнаружено прямое токсическое действие арсина на почечные клеточные линии в культуре..
Физико-химическая характеристика
Физические характеристики
| Молекулярная масса (усл. ед.) | 77,95 | Температура кипения (С) | -62,5 |
| Плотность пара по воздуху | 2,69 | Температура плавления (С) | -116,9 |
| Плотность (г/м3) | 1,34 | Температура разрушения (С) | 280 |
| Скорость испарения (кг*с/м3) | 0,0544 | Удельная теплота парообразования (кДж/кг) | 214 |
| Давление пара (мм рт.ст.) при ну | Удельная теплоёмкость жидкости (кДж/кг*С) | 0,494 | |
| Запах | слабый, чесночный | Термостабильность | легко разлагается при нагревании |
Методы индикации
В воздухе: колориметрический метод, основан на окислении арсина до мышьяковисто кислоты с последующим взаимодействием ее с молибдатом аммония с образованием молибденового комплекса, окрашивающего раствор в синий цвет; нижний предел обнаружения арсина 0,2 мкг в анализируемом объеме, измеряемые концентрации 0,01-0,05 мг/куб.м.
Химические свойства
Арсин проявляет сильные восстановительные свойства, например, из раствора нитрата серебра он осаждает металлическое серебро:
-
- AsH3+6AgNO3+3H2O→6Ag↓+As(OH)3+6HNO3{\displaystyle {\mathsf {AsH_{3}+6AgNO_{3}+3H_{2}O\rightarrow 6Ag\downarrow +As(OH)_{3}+6HNO_{3}}}}
Арсин сравнительно нестоек и медленно разлагается даже при комнатной температуре на водород и элементарный мышьяк, при температуре 500 °C — мгновенно:
-
- 2AsH3→2As+3H2{\displaystyle {\mathsf {2AsH_{3}\rightarrow 2As+3H_{2}}}}
- При пропускании AsH3 через нагретую, наполненную водородом стеклянную трубку, металлический мышьяк отлагается на стенках трубки в виде черно-бурого зеркала. На этом свойстве арсина основана высокочувствительная качественная реакция на мышьяк — проба Марша.
Не самовоспламеняется на воздухе и в кислороде при комнатной температуре, но при нагревании на воздухе до 200 °C сгорает:
-
- 2AsH3+3O2→As2O3+3H2O{\displaystyle {\mathsf {2AsH_{3}+3O_{2}\rightarrow As_{2}O_{3}+3H_{2}O}}}
В хлоре самовоспламеняется даже при −196оС, с замещением водорода на хлор и выделением хлороводорода:
-
- AsH3+3Cl2→AsCl3+3HCl{\displaystyle {\mathsf {AsH_{3}+3Cl_{2}\rightarrow AsCl_{3}+3HCl}}}
- С бромом и йодом реагирует таким же образом, давая соответствующие галогениды.
С серой реагирует:
-
- 2AsH3+3S→3H2S+2As{\displaystyle {\mathsf {2AsH_{3}+3S\rightarrow 3H_{2}S+2As}}}
Реагирует с концентрированной соляной кислотой c выделением водорода:
-
- AsH3+3HCl→AsCl3+3H2{\displaystyle {\mathsf {AsH_{3}+3HCl\rightarrow AsCl_{3}+3H_{2}}}}
Реагирует с растворами щелочных металлов в жидком аммиаке, проявляя кислотные свойства и образуя мышьяковистые производные, аналогичные амидам щелочных металлов:
-
- AsH3+NaNH2→NaAsH2+NH3{\displaystyle {\mathsf {AsH_{3}+NaNH_{2}\rightarrow NaAsH_{2}+NH_{3}}}}
При нагревании арсина с металлами образуются арсениды.
Структура арсина
Как видно из двух изображений выше, AsH3 Имеет пирамидальную структуру. Атом As находится в центре пирамиды, а три H в каждой из ее вершин. Химическая гибридизация As должна быть обычно3 принять эту геометрию.
На изображении видно, что связи As-H имеют длину 1,519 Å, а три Н разделены углом 91,8º. Этот угол значительно отличается от 107º для молекулы аммиака, NH3, указывая на приближение между H.
Некоторые химики утверждают, что это связано с различием атомных радиусов между N и Ace.
Будучи наименьшим N, H находятся ближе друг к другу, увеличивая их электростатические отталкивания, которые имеют тенденцию отталкивать их. Между тем, туз больше, поэтому Н более удалены друг от друга, а отталкивания между ними меньше, поэтому они имеют тенденцию отделяться меньше.
АРСИНЕ: число душевных стремлений «8»
Восемь – число устремлений души, придающее человеку громадное желание независимости. Для таких людей не существует авторитетов. Собственные мысли и идеалистические представления о мире делают их изгоями и отщепенцами. Однако громадная целеустремленность и умение диктовать собственные правила приводят людей «восьмерки» к признанию и заслуженному лидерству в коллективе.
Жажды власти, богатства и славы предостаточно
Желая обеспечить достойный уровень жизни для своего семейства, человек числа восемь может ступить на опасный путь, но природная осторожность не даст пострадать от собственной неосмотрительности. Чем раньше такой человек найдет наиболее подходящее дело для себя, тем скорее он приобретет авторитет, и тем более размеренной будет его жизнь
Если такого не происходит, то «восьмерочник» погружается в борьбу со стереотипами, предубеждениями, нормами и кажущейся несправедливостью. Вечный бой лишает людей числа восемь сил и бодрости, а также вероятности найти свое счастье. «Восьмерочники» часто имеют способности предпринимателя, но своими деньгами не рискуют. Их бизнес успешен, а партнеры и инвесторы честны.
Удача сопутствует людям восьмерки только тогда, когда выбрано правильное направление для самовыражения и реализации. Жизнь только своими интересами приводит к тоске, унынию и одиночеству, но эгоизм угасает, как только приходит понимание, что чем больше отдаешь, тем больше приобретаешь.
Люди числа восемь имеют огромные амбиции, но не всегда находят силы для их воплощения. Умение убеждать, увлечь за собой других открывает соратникам немалые возможности, однако чересчур трудный выбор ведущего наказывается своими же единомышленниками ударом в спину. Находчивость помогает сориентироваться в сложной ситуации, а речь, подкрепленная обоснованными аргументами, вызывает безграничное доверие.
Самый худший вариант «восьмерочника» нетерпелив, лишен благоразумия, капризен и невероятно придирчив в любовных отношениях, но даже такой всегда прислушивается к голосу разума и пересмотрит свои поступки, если убедится, что так надо для исполнения задуманного.
Токсичность и опасность
Воздух рабочей зоны
| ПДК максимальная разовая, мг/м3 | 0,1 |
| Класс опасности | 1 |
| Особенности токсического действия вещества на организм | остронаправленный механизм действия, требующий автоматического контроля за содержанием вещества в воздухе (О) |
Аварийные гигиенические регламенты и референтные уровни
| Уровни острой ингаляционной
экспозиции (мг/м³) |
|
||||||||||||||||||||||||
| Аварийные пределы воздействия
отравляющих веществ в воздухе (АПВ, мг/м³) |
|
||||||||||||||||||||||||
| Референтные концентрации для
хронического ингаляционного |
5E-05 | ||||||||||||||||||||||||
| Поражаемые органы и системы | кровь, сердечно-сосудистая система, селезенка | ||||||||||||||||||||||||
| Субъективная реакция дискомфорта (мг/м³) |
14 |
Опасность при утечке
Вещество может всасываться в организм при вдыхании. При утечке содержимого очень быстро достигается опасная концентрация этого газа в воздухе. Вдыхание газа может вызвать отек легких. Быстрое испарение жидкости может вызвать обморожение. Вещество может оказывать действие на кровь и почки , приводя к повреждению кровяных клеток и поражению почек. Вещество разлагается при разогреве и под влиянием света и влажности с образованием токсичных паров мышьяка. Реагирует бурно с сильными окислителями, фтором, хлором, азотной кислотой, трихлоридом азота с опасностью пожара и взрыва. Газ тяжелее воздуха. и может стелиться по земле; возможно возгорание на расстоянии. В результате вытекания, перемешивания и др. могут образоваться электростатические заряды.
Острая токсичность
| Токсичность для животных |
|
||||||||
|
Токсичность для человека |
| Тип дозы | Способ измерения | Механизм воздействия | Состояние человека | Значение |
|---|---|---|---|---|
|
Наименьшая опубликованная смертельная доза (LCLo, LDLo) |
в целом на организм | ингаляционно | в состоянии покоя | 78,7 (30 мин) мг/м3 |
|
Наименьшая опубликованная смертельная доза (LCLo, LDLo) |
в целом на организм | ингаляционно | в состоянии покоя | 944 (5 мин) мг/м3 |
| Наименьшая опубликованная токсичная доза (TCLo, TDLo) | в целом на организм | ингаляционно | в состоянии покоя | 0,325 мг/м3 |
| Мгновенно-опасная для жизни или здоровья концентрация (IDLH) | в целом на организм | ингаляционно | в состоянии покоя | 9447 мг/м3 |
| Пороговая токсодоза (PCt50, мг.мин/л) | 0,02 |








