Дисульфид углерода
Содержание:
- Последствия отравления сероуглеродом
- Свойства
- Первая помощь и лечение отравления соединениями серы
- Примечания
- Моль
- Химические свойства углерода
- definition — Сероуглерод
- Сероуглерод
- Свойства
- Получение
- Применение
- Токсическое действие
- Первая помощь и лечение
- Физические свойства
- Очищение
- Первая помощь и неотложная терапия
- Применение сероуглерода
- Применение
Последствия отравления сероуглеродом
Доказано, что в результате нарушения окислительных процессов, вызываемых сероуглеродом, уменьшается образование важного витамина Вб, который участвует в регуляции жирового обмена. В результате повышается содержание общего холестерина и снижается содержание свободных жирных кислот
А это – одно из условий атеросклеротического изменения сосудов.
Ряд исследователей полагают, что сероуглерод является скорее не нервным, а сосудистым ядом. Однако в этом вопросе нет единого мнения.
Отравление сероуглеродом способствует развитию еще одного распространенного заболевания – сахарного диабета. Самые ранние признаки его может обнаружить только врач, так как они незаметны для больного. И даже не один врач, а специалисты нескольких профилей. Поэтому в профилактических осмотрах людей, имеющих производственный контакт с сероуглеродом, должны принимать участие невропатолог, терапевт, окулист, а при необходимости и психиатр.
Каковы же симптомы отравления сероуглеродом? Острые заболевания крайне редки (наблюдаются лишь вследствие аварийных ситуаций), так как в условиях современного производства пары сероуглерода в воздухе редко достигают высоких концентраций.
Хроническое отравление сероуглеродом
развивается через много лет работы в контакте с небольшими дозами сероуглерода. Легкая степень отравления напоминает алкогольное опьянение: возбужденное состояние с болтливостью, немотивированными поступками, эйфорией, головными болями, тошнотой. Затем эйфория сменяется депрессией и сонливостью. Такой период эмоциональной неустойчивости сменяется астеновегетативным синдромом. Значительно изменяется психика: появляется забывчивость, теряется интерес к жизни, развлечениям, ослабляется привязанность к близким людям. Могут быть эпизоды резкой вспыльчивости, необоснованной тревоги. Все эти признаки укладываются в картину «сероуглеродного невроза».
Сероуглерод летуч. Проникая в организм преимущественно через дыхательные пути, он захватывается кровью, задерживается тканью, особенно богатой жиром (благодаря своей способности в нём растворяться). Частично сероуглерод выводится в неизменном виде с мочой, а также в виде соединений, содержащих серу.
Из этого следует, что для диагностики важно определение этого яда и его соединений в крови или моче
Свойства
Чистый сероуглерод представляет собой бесцветную жидкость с приятным «эфирным» запахом. Технический продукт, полученный сульфидированием угля, имеет неприятный «редечный» запах. Молекула CS2 линейна, длина связи С—S = 0,15529 нм; энергия диссоциации 1149 кДж/моль.
Сероуглерод токсичен, огнеопасен, имеет самый широкий диапазон концентрационных пределов взрываемости.
- CS2+3O2→CO2+2SO2{\displaystyle {\mathsf {CS_{2}+3O_{2}\rightarrow CO_{2}+2SO_{2}}}}
Подобно диоксиду углерода, CS2 является кислотным ангидридом и при взаимодействии с некоторыми сульфидами может образовывать соли тиоугольной кислоты (Н2СS3). При реакции с щелочами образуются соли дитиоугольной кислоты и продукты их диспропорционирования.
Однако сероуглерод, в отличие от диоксида углерода, проявляет большую реакционную способность по отношению к нуклеофилам и легче восстанавливается.
Так, сероуглерод способен реагировать с C-нуклеофилами, его взаимодействие с енолятами активированных метиларилкетонов идет с образованием бис-тиолятов арилвинилкетонов, которые могут быть проалкилированы до бис-алкилтиоарилвинилкетонов; эта реакция имеет препаративное значение:
-
- PyCOCH3+CS2+2t-BuOK→PyCOCH=C(S−K+)2+2t-BuOH{\displaystyle {\mathsf {PyCOCH_{3}+CS_{2}+2t{\text{-}}BuOK\rightarrow PyCOCH{\text{=}}C(S^{-}K^{+})_{2}+2t{\text{-}}BuOH}}}
-
- PyCOCH=C(S−K+)+2MeI→PyCOCH=C(SMe)2+2KI{\displaystyle {\mathsf {PyCOCH{\text{=}}C(S^{-}K^{+})+2MeI\rightarrow PyCOCH{\text{=}}C(SMe)_{2}+2KI}}}
При взаимодействии с натрием в диметилформамиде сероуглерод образует 1,3-дитиол-2-тион-4,5-дитиолят натрия, использующийся в качестве предшественника в синтезе тетратиафульваленов:
При взаимодействии с первичными или вторичными аминами в щелочной среде образуются соли дитиокарбаматы:
- 2R2NH+CS2→R2NH2+R2NCS2−{\displaystyle {\mathsf {2R_{2}NH+CS_{2}\rightarrow }}}
Для растворимых дитиокарбаматов характерно образование комплексов с металлами, что используется в аналитической химии. Они также имеют большое промышленное значение в качестве катализаторов вулканизации каучука.
Со спиртовыми растворами щелочей образует ксантогенаты:
- RONa+CS2→Na+ROCS2−{\displaystyle {\mathsf {RONa+CS_{2}\rightarrow }}}
Такими сильными окислителями, как, например, перманганат калия, сероуглерод разлагается с выделением серы.
С оксидом серы (VI) сероуглерод взаимодействует с образованием сульфоксида углерода:
- CS2+3SO3→COS+4SO2{\displaystyle {\mathsf {CS_{2}+3SO_{3}\rightarrow COS+4SO_{2}}}}
С оксидом хлора(I) образует фосген:
- CS2+3Cl2O→COCl2+2SOCl2{\displaystyle {\mathsf {CS_{2}+3Cl_{2}O\rightarrow COCl_{2}+2SOCl_{2}}}}
Сероуглерод хлорируется в присутствии катализаторов до перхлорметилмеркаптана CCl3SCl, использующегося в синтезе тиофосгена CSCl2:
- 2CS2+5Cl2→2CCl3SCl+S2Cl2{\displaystyle {\mathsf {2CS_{2}+5Cl_{2}\rightarrow 2CCl_{3}SCl+S_{2}Cl_{2}}}}
- CCl3SCl→HCSCl2+2HCl{\displaystyle {\mathsf {CCl_{3}SCl{\xrightarrow{}}CSCl_{2}+2HCl}}}
Избытком хлора сероуглерод хлорируется до четырёххлористого углерода:
- CSCl2+2Cl2→CCl4+S2Cl2{\displaystyle {\mathsf {CSCl_{2}+2Cl_{2}\rightarrow CCl_{4}+S_{2}Cl_{2}}}}
Фторирование сероуглерода фторидом серебра в ацетонитриле ведет к образованию трифторметилтиолята серебра, эта реакция имеет препаративное значение
При температурах выше 150 °C протекает гидролиз сероуглерода по реакции:
- CS2+2H2O→CO2+2H2S{\displaystyle {\mathsf {CS_{2}+2H_{2}O\rightarrow CO_{2}+2H_{2}S}}}
Первая помощь и лечение отравления соединениями серы
Антидотом серы выступает Атропин, его применяют, как правило, при интоксикации парами вещества.
При отравлении любыми соединениями серы в первую очередь необходимо немедленно вывести пострадавшего на свежий воздух. Для промывания глаз, слизистых, полоскания носа и горла можно использовать 2% раствор соды (примерно полчайной ложки на 200 мл воды).
Сероуглерод
- Если состояние больного тяжелое, до приезда скорой внутривенно можно ввести раствор глюкозы с аскорбиновой кислотой, витамином B6 (5 мл, 5% р-р), глютаминовую кислоту (20 мл, 1% р-р).
- Как было описано выше, сероуглерод отличается своим воздействием на ЦНС, что требует специфичного лечения, направленного на нормализацию обменных процессов мозга, подавление повышенной нервной возбудимости посредством транквилизаторов.
- В случае хронического отравления больным необходимо комплексное лечение под строгим наблюдением медиков.
Сернистый газ
- Чтобы уменьшить раздражение глаз следует капнуть раствором Левомицетина (0,25%), надеть на больного солнцезащитные очки.
- Для облегчения дыхания и снижения воспаления в нос необходимо закапать сосудосуживающие средства (например, Фармазолин).
- Развитие последующих инфекций (на фоне пораженной носоглотки) предотвращает применение аэрозоля антибиотиков с сульфаниламидами в растворе новокаина.
- Предупреждает отек легких введение в вену хлорида кальция с глюкозой (20 мл, 40% р-р) с аскорбиновой кислотой (1 мл, 5% р-р).
- Если развивается спазм гортани, в вену вводится сульфат атропина (1 мл, 0,1% р-р).
Примечания
- Относительная электроотрицательность атома углерода зависит от состояния его гибридизации: Csp3 = 2,5 (в большинстве таблиц) Csp2 = 2,8 Csp1 = 3,2 (алкины)С. Э. Зурабян, Ю. А. Колесник, А. А. Кост и др./под ред. Н. А. Тюкавкиной. Взаимное влияние атомов в молекуле // Органическая химия: Учебник (Учеб. лит. Для учащихся фарм. училищ). — М.: Медицина, 1989. — Т. 1. — С. 36. — 432 с. — ISBN 5-225-00314-1.
-
(англ.) (недоступная ссылка). Дата обращения 6 декабря 2007.
-
(англ.) (недоступная ссылка). Дата обращения 6 декабря 2007.
-
(англ.). Дата обращения 6 декабря 2007.
- ↑ Savvatimskiy, A (2005). «Measurements of the melting point of graphite and the properties of liquid carbon (a review for 1963–2003)». Carbon. 43 (6): 1115–1142. doi:10.1016/j.carbon.2004.12.027
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
-
.
- Лейпунский О. И. Об искусственных алмазах (рус.) // Успехи химии. — Российская академия наук, 1939. — Вып. 8. — С. 1519—1534.
- Seal M. The effect of surface orientation on the graphitization of diamond. // Phis. Stat. Sol., 1963, v. 3, p. 658.
- Evans T. Changes produced by High Temperature Treatment of Diamond. // The Properties of Diamond. Academi Press, 1979, p. 403–424.
- Андреев В. Д.. Спонтанная графитизация и термодеструкция алмаза при Т > 2000 K // Физика твердого тела, 1999, т. 41, вып. 4, с. 695—201.
- Togaya M. Melting behaviors of carbon underhigh pressure // High Pressure Research, 1990, v. 4, p. 342. (12 AIRAPT Conf. Proc., 1989, Padeborn).
- Андреев В. Д.. Экспериментальные данные по плавлению алмаза и графита с учетом аномальности высокотемпературной теплоёмкости // Химическая физика, 2002, т. 21, № 9, с. 3—11.
- ↑
-
. РИА Новости (20190514T1558+0300Z). Дата обращения 14 мая 2019.
-
. ТАСС. Дата обращения 14 мая 2019.
-
. indicator.ru. Дата обращения 14 мая 2019.
- V. I. Kasatochkin, A. M. Sladkov, et al., Dokl. Akad. Nauk SSSR, 177, No. 2, 358 (1967).
- Р. А. Лидин. Химические свойства неорганических веществ. — Третье. — 2004. — С. 100. — 162 с.
-
Минфин РФ. . minfin.ru (27 февраля 2015). — Статистические данные по добыче природных алмазов с 01.01.2003 по 31.12.2014 по результатам сортировки и первичной оценки. Дата обращения 28 июня 2015.
Моль
Все вещества состоят из атомов и молекул
В химии важно точно измерять массу веществ, вступающих в реакцию и получающихся в результате нее. По определению моль является единицей количества вещества в СИ
Один моль содержит точно 6,02214076×10²³ элементарных частиц. Это значение численно равно константе Авогадро NA, если выражено в единицах моль⁻¹ и называется числом Авогадро. Количество вещества (символ n) системы является мерой количества структурных элементов. Структурным элементом может быть атом, молекула, ион, электрон или любая частица или группа частиц.
Постоянная Авогадро NA = 6.02214076×10²³ моль⁻¹. Число Авогадро — 6.02214076×10²³.
Другими словами моль — это количество вещества, равное по массе сумме атомных масс атомов и молекул вещества, умноженное на число Авогадро. Единица количества вещества моль является одной из семи основных единиц системы СИ и обозначается моль. Поскольку название единицы и ее условное обозначение совпадают, следует отметить, что условное обозначение не склоняется, в отличие от названия единицы, которую можно склонять по обычным правилам русского языка. Один моль чистого углерода-12 равен точно 12 г.
Химические свойства углерода
Углерод способен образовывать несколько аллотропных модификаций. Это алмаз (наиболее инертная аллотропная модификация), графит, фуллерен и карбин.
Древесный уголь и сажа представляют собой аморфный углерод. Углерод в таком состоянии не имеет упорядоченной структуры и фактически состоит из мельчайших фрагментов слоев графита. Аморфный углерод, обработанный горячим водяным паром, называют активированным углем. 1 грамм активированного угля из-за наличия в нем множества пор имеет общую поверхность более трехсот квадратных метров! Благодаря своей способности поглощать различные вещества активированный уголь находит широкое применение как наполнитель фильтров, а также как энтеросорбент при различных видах отравлений.
С химической точки зрения аморфный углерод является наиболее активной его формой, графит проявляет среднюю активность, а алмаз является крайне инертным веществом. По этой причине, рассматриваемые ниже химические свойства углерода следует прежде всего относить к аморфному углероду.
Восстановительные свойства углерода
Как восстановитель углерод реагирует с такими неметаллами как, например, кислород, галогены, сера.
В зависимости от избытка или недостатка кислорода при горении угля возможно образование угарного газа CO или углекислого газа CO2:
При взаимодействии углерода со фтором образуется тетрафторид углерода:
При нагревании углерода с серой образуется сероуглерод CS2:
Углерод способен восстанавливать металлы после алюминия в ряду активности из их оксидов. Например:
Также углерод реагирует и с оксидами активных металлов, однако в этом случае наблюдается, как правило, не восстановление металла, а образование его карбида:
Взаимодействие углерода с оксидами неметаллов
Углерод вступает в реакцию сопропорционирования с углекислым газом CO2:
Одним из наиболее важных с промышленной точки зрения процессов является так называемая паровая конверсия угля. Процесс проводят, пропуская водяной пар через раскаленный уголь. При этом протекает следующая реакция:
При высокой температуре углерод способен восстанавливать даже такое инертное соединение как диоксид кремния. При этом в зависимости от условия возможно образование кремния или карбида кремния (карборунда):
Также углерод как восстановитель реагирует с кислотами окислителями, в частности, концентрированными серной и азотной кислотами:
Окислительные свойства углерода
Химический элемент углерод не отличается высокой электроотрицательностью, поэтому образуемые им простые вещества редко проявляют окислительные свойства по отношению к другим неметаллам.
Примером таких реакций является взаимодействие аморфного углерода с водородом при нагревании в присутствии катализатора:
а также с кремнием при температуре 1200-1300 оС:
Окислительные свойства углерод проявляет по отношению к металлам. Углерод способен реагировать с активными металлами и некоторыми металлами средней активности. Реакции протекают при нагревании:
Карбиды активных металлов гидролизуются водой:
а также растворами кислот-неокислителей:
При этом образуются углеводороды, содержащие углерод в той же степени окисления, что и в исходном карбиде.
definition — Сероуглерод
of Wikipedia
Advertizing ▼
Wikipedia
Сероуглерод
Материал из Википедии — свободной энциклопедии
Перейти к: ,
| Сероуглерод | |
| Carbon-disulfide-2D-dimensions.png | |
| Carbon-disulfide-3D-vdW.png | |
| Общие | |
|---|---|
| Систематическое наименование | Сероуглерод |
| Химическая формула | CS2 |
| Отн. молек. масса | 76.1 а. е. м. |
| Молярная масса | 76.1 г/моль |
| Физические свойства | |
| Состояние () | бесцветная жидкость |
| Плотность | 1.26 г/см³ |
| Термические свойства | |
| Температура плавления | -111.6 °C |
| Температура кипения | 46 °C |
| () | 89,41 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 0.2 г/100 мл |
| Классификация | |
| Рег. номер CAS | |
| SMILES | CS(S) |
Сероуглерод CS2 — соединение серы с углеродом, бесцветная жидкость с неприятным запахом. Молекула CS2 линейна, длина связи С—S = 0,15529 нм; энергия диссоциации 1149 кДж/моль.
Свойства
Пары его ядовиты и очень легко воспламеняются. Сгорание их идет по уравнению:
- CS2 + 3О2 = СО2 + 2SO2
При температурах выше 150 °С протекает гидролиз сероуглерода по реакции:
- CS2 + 2H2O → CO2 +2H2S
Подобно диоксиду углерода, CS2 является кислотным ангидридом и при взаимодействии с некоторыми сульфидами может образовывать соли тиоугольной кислоты (Н2СS3).
Однако, сероуглерод, в отличие от диоксида углерода, проявляет большую реакционную способность по отношению к нуклеофилам и легче восстанавливается. Такими сильными окислителями, как, например, перманганат калия, сероуглерод разлагается с выделением серы.
С оксидом серы (VI) сероуглерод взаимодействует с образованием серооксида углерода:
- CS2 + 3SO3 → COS + 4SO2;
С оксидом хлора(I) образует фосген:
- CS2 + 3Cl2O → COCl2 + 2SOCl2
При взаимодействии с первичными или вторичными аминами в щелочной среде, образуются соли дитиокарбаматы:
- 2R2NH + CS2 → [R2NH2+][R2NCS2−]
Для растворимых дитиокарбоматов характерно образование комплексов с металлами. Они также имеют большое промышленное значение в качестве катализаторов вулканизации каучука.
Со спиртовыми растворами щелочей образует ксантогенаты:
- RONa + CS2 → [ROCS2−]
Серуглерод хлорируется в присутствии катализаторов:
- CS2 + 3Cl2 → CCl4 + S2Cl2
Получение
В промышленности получают по реакции СН4 с парами серы в присутствии силикагеля при 500-700 °С в камере из хромоникелевой стали:
- CH4 + ½S8 → CS2 + 2H2S
Также сероуглерод можно получить взаимодействием древесного угля и паров S при 750-1000 °С.
Применение
Хорошо растворяет жиры, масла, смолы, каучук; растворяет серу, фосфор, иод, нитрат серебра. Большая часть (80%) производимого сероуглерода идет в производство искусственного шелка — вискозы. Его применяют для получения различных химических веществ (ксантогенатов, четыреххлористого углерода, роданидов). Сероуглерод используют как экстрагент, применяют при вулканизации каучука.
Токсическое действие
Смертельная доза при поступлении внутрь составляет 1 г. Высокотоксичная концентрация в воздухе — свыше 10 мг/л. Оказывает местное раздражающее, резорбтивное действия. Обладает психотропными, нейротоксическими свойствами, которые связаны с его наркотическим воздействием на центральную нервную систему.При отравлении возникают головная боль, головокружение, судороги, потеря сознания. Бессознательное состояние может сменяться психическим и двигательным возбуждением. Могут наблюдаться рецидивы судорог с потерей сознания, угнетение дыхания. При приеме внутрь наступают тошнота, рвота, боли в животе.При контакте с кожей наблюдаются гиперемия и химические ожоги.
Первая помощь и лечение
Прежде всего, необходимо удалить пострадавшего из пораженной зоны.При попадании сероуглерода внутрь необходимо выполнить промывание желудка с использованием зонда, форсированный диурез, ингаляцию кислорода.Обычно проводится симптоматическую терапию. При судорогах вводят 10 мг. диазепама внутривенно.
| Это незавершённая статья о неорганическом соединении. Вы можете помочь проекту, исправив и дополнив её. |
Физические свойства
Углерод существует во множестве аллотропных модификаций с очень разнообразными физическими свойствами. Разнообразие модификаций обусловлено способностью углерода образовывать химические связи разного типа.
Изотопы углерода
Основная статья: Изотопы углерода
Природный углерод состоит из двух стабильных изотопов — 12С (98,93 %) и 13С (1,07 %) и одного радиоактивного изотопа 14С (β-излучатель, Т½ = 5730 лет), сосредоточенного в атмосфере и верхней части земной коры. Он постоянно образуется в нижних слоях стратосферы в результате воздействия нейтронов космического излучения на ядра азота по реакции: 14N (n, p) 14C, а также, с середины 1950-х годов, как техногенный продукт работы АЭС и в результате испытания водородных бомб.
На образовании и распаде 14С основан метод радиоуглеродного датирования, широко применяющийся в четвертичной геологии и археологии.
Очищение
Сероуглерод, полученный вышеописанными способами, содержит в растворе 10-12 % серы, сероводород и различные сернистые органические вещества. Чтобы очистить сырой С., его подвергают перегонке и обрабатывают различными реагентами: щелочами, белильной известью, азотно-свинцовой солью и пр. Очищение С. сопровождается большими потерями его (до 25 %). Боньер производит перегонку сероводорода в серии котлов В В В B (фиг. 3).
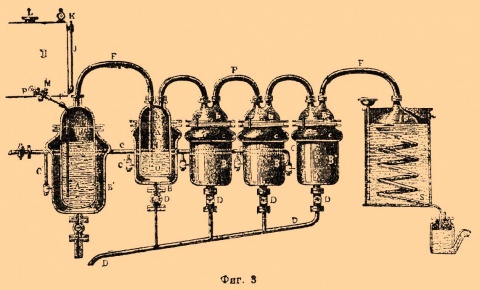 Фиг. 3.
Фиг. 3.
Котлы делаются с двойными стенками; между последними циркулирует пар, который берется из паропровода С и ведется к каждому котлу при помощи отростков C. Конденсационная вода спускается из котлов через краны D в общую сточную трубу D. Котел А наполняется крепким раствором едкого кали и нагревается до 60-65°; в него при помощи трубки P напускается С. из хранителя Н; количество С. определяется по водомерной трубке J. Котлы B двугорлые; они наполнены частью щелочью, частью растворами солей свинца, меди и железа и соединены между собой трубопроводами F, идущими от верхушки шлема одного котла до дна следующего. Пары С. по трубе F идут из одного котла в нижнюю часть другого, проходят через слой промывочной жидкости и, наконец, поступают в холодильник S, где и сгущаются. Дейсс перегоняет С. в большом железном котле, который до 2/3 наполняется С.; сюда приливают несколько литров щелочи, хлорной воды или раствора белильной извести; котел нагревается паром, причем гонку ведут очень медленно. По Зингеру, сырой С. обрабатывается в цилиндре (2 м высоты и 0,7 м диам.) прозрачным известковым раствором, который впрыскивается в него при помощи свинцовой дырчатой трубки, лежащей на дне цилиндра; обработка кончается, когда вытекающий сверху цилиндра известковый раствор оказывается прозрачным. К промытому таким образом С. прибавляют 1 % жира и перегоняют на водяной бане, покрыв С. слоем воды в 1 стм. Для получения химически чистого С. из продажного Клоез советует взбалтывать его с ½ % сулемы и перегонять, прибавив 2 % бесцветного жира. Сидо взбалтывает его перед перегонкой с ртутью. По Обаху, для окончательного очищения С. поступают следующим образом: продажный С. процеживают через фильтр в колбу с негашеной известью, оставляют на некоторое время и затем отгоняют (не до конца) на водяной ванне, которая держится при 60-70°. Дистиллят взбалтывают с грубо измельченным порошком марганцово-калиевой соли (5 г на 1 литр С.) и оставляют стоять, пока не исчезнет запах сероводорода; затем С. сливают и сначала сильно взбалтывают с несколькими граммами чистой ртути, а потом с сернокислой ртутью (25 г на 1 л. CS 2), пока не исчезнет редечный запах. После такой обработки С. сливают в колбу с хлористым кальцием (пористым), откуда его перегоняют (не на свету) в сухие склянки, где он и хранится в темноте.
Первая помощь и неотложная терапия
Пострадавшего необходимо немедленно удалить из помещения, забоя и др. с опасной концентрацией С., перенести или перевести в теплое, проветриваемое помещение или на свежий воздух, освободить от стесняющей дыхание одежды. Необходимы покой, грелки, рефлекторное возбуждение дыхания, вдыхание кислорода; при коматозном состоянии — средства, стимулирующие дыхание и сердечную деятельность (цититон, лобелин, кофеин, стрихнин, витамины С, B6, B15). При двигательном возбуждении вводят хлоралгидрат в микроклизме. Пострадавшего необходимо как можно скорее госпитализировать. Дальнейшее лечение — симптоматическое.
Экспертиза трудоспособности
. В начальных стадиях хрон. интоксикации С. трудоспособность больных чаще всего сохранена. Переводу на работы, исключающие контакт с С., подлежат лица со стойкими функциональными нарушениями нервной системы, а также с полиневропатией при отсутствии эффекта от лечения. Показанием к определению III группы инвалидности или частичной утраты профессиональной трудоспособности у таких больных часто служит затруднение в трудоустройстве, поскольку при продолжении контакта с С. наступающее у них нарушение гомеостаза может носить прогрессирующий характер.
Профилактические меры
. Обязательна механизация работ, сопряженных с контактом с С., герметизация оборудования, использование средств индивидуальной защиты — промышленные противогазы (см.) в условиях повышенного содержания паров С. в воздухе рабочей зоны, при очень высоких концентрациях С. в воздухе — кислородные приборы. Обязательна защита кожи — резиновые перчатки, фартуки, галоши (см. Обувь , Одежда специальная) — и глаз (см. Очки).
Необходимо периодическое проведение медицинских осмотров (см. Медицинский осмотр). Большое значение имеет также лечение сопутствующих заболеваний, что способствует общему снижению проф. заболеваемости работающих в контакте с С.
Предельно допустимая концентрация сероуглерода в воздухе рабочей зоны — 1 мг/м 3 .
Применение сероуглерода
Сфера применения в промышленности сероуглерода сейчас довольно широка. Он используется как растворитель жиров, резины и фосфора. Всем известный целлофан не вырабатывается без его помощи. Сероуглерод применяется как инсектицид, используется он и в вискозной промышленности.
Многолетний контакт даже с очень, незначительными квонцентрациями сероуглерода способствует раннему развитию атеросклероза с преимущественным поражением сосудов мозга и почек
Отсюда очевидна важность знания ранних признаков отравления этим ядом. Здесь опять заметна тесная взаимосвязь профессиональных и внутренних болезней
Поэтому подробное изучение механизма воздействия сероуглерода помогает познавать тайны опасной и незаметно подкрадывающейся болезни – атеросклероза. А там, где известны причины заболевания, уже можно подобрать ключ к его устранению.
Применение
Графит используют в карандашной промышленности, но в смеси с глиной, для уменьшения его мягкости. Также его используют в качестве смазки при особо высоких или низких температурах. Его невероятно высокая температура плавления позволяет делать из него тигли для заливки металлов. Способность графита проводить электрический ток также позволяет изготавливать из него высококачественные электроды.
Алмаз благодаря исключительной твёрдости — незаменимый абразивный материал. Алмазным напылением обладают шлифовальные насадки бурмашин. Кроме этого, огранённые алмазы — бриллианты — используются в качестве драгоценных камней в ювелирных украшениях. Благодаря редкости, высоким декоративным качествам и стечению исторических обстоятельств бриллиант неизменно является самым дорогим драгоценным камнем. Исключительно высокая теплопроводность алмаза (до 2000 Вт/м·К) делает его перспективным материалом для полупроводниковой техники в качестве подложек для процессоров. Но относительно высокая себестоимость добычи алмазов ($97,47 за один карат) и сложность обработки алмаза ограничивают его применение в этой области.
В фармакологии и медицине широко используются различные соединения углерода: производные угольной кислоты и карбоновых кислот, различные гетероциклы, полимеры и другие соединения. Так, карболен (активированный уголь), применяется для абсорбции и выведения из организма различных токсинов; графит (в виде мазей) — для лечения кожных заболеваний; радиоактивные изотопы углерода — для научных исследований (радиоуглеродный анализ).
Углерод играет огромную роль в жизни человека. Его применения столь же разнообразны, как сам этот многоликий элемент. В частности, углерод является неотъемлемой составляющей стали (до 2,14 % масс.) и чугуна (более 2,14 % масс.)
Углерод является основой всех органических веществ. Любой живой организм состоит в значительной степени из углерода. Углерод — основа жизни. Источником углерода для живых организмов обычно является СО2 из атмосферы или воды. В результате фотосинтеза он попадает в биологические пищевые цепи, в которых живые существа поедают друг друга или останки друг друга и тем самым добывают углерод для строительства собственного тела. Биологический цикл углерода заканчивается либо окислением и возвращением в атмосферу, либо захоронением в виде угля или нефти.
Углерод в виде ископаемого топлива: угля и углеводородов (нефть, природный газ) — один из важнейших источников энергии для человечества.










