Этилмеркаптан
Содержание:
Биологическая роль
Смесь тиолов содержится в веществе, выделяемом скунсами, а также в продуктах гниения белков.
Аминокислота цистеин HSCH2CH(NH2)COOH, содержащая меркаптогруппу, входит в состав всех белков, а окисление цистеина с образованием дисульфидных мостиков в ходе посттрансляционной модификации белков является важнейшим фактором при формировании их третичной структуры. Высокая механическая прочность кератинов обусловлена, в том числе, и высокой степенью сшитости за счёт образования большого количества дисульфидных мостиков: так, например, содержание цистеина в кератине волоса человека, составляет ~14 %, а в некоторых кератинах доля цистеина может достигать и 30 %.
Трипептид глутатион, в состав которого также входит цистеин, является коферментом глутатионпероксидаз и играет важную роль в окислительно-восстановительных процессах в живых организмах.
Также существенное биологическое значение имеет метаболическое нитрозирование тиолов: глутатион и цистеиновые остатки белков при взаимодействии с активными формами азота образуют S-нитрозопроизводные, которые являются физиологическим депо оксида азота.
Химические свойства
Кислотность
Тиолы являются слабыми кислотами, образуя с гидроксидами щелочных и щелочноземельных металлов растворимые в воде тиоляты (меркаптиды), с солями тяжелых металлов — нерастворимые меркаптиды. Являются значительно более сильными кислотами, чем соответствующие кислородные спирты.
|
|
|
|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
н-C3H7SH |
|
|
трет-C4H9SH |
|
Тиолят-анионы высоконуклеофильны, и многие реакции замещения водорода группы -SH протекают через промежуточное образование тиолятов.
Так, тиолы алкилируются под действием алкилгалогенидов:
-
- RS−+R1Hal→RSR1+Hal−{\displaystyle {\mathsf {RS^{-}+R^{1}Hal\rightarrow RSR^{1}+Hal^{-}}}}
Тиолы в присутствии оснований (пиридина, третичных аминов) ацилируются с образованием S-ацилпроизводных:
-
- RSH+R1C(O)Hal→R1C(O)SR+HX{\displaystyle {\mathsf {RSH+R^{1}C(O)Hal\rightarrow R^{1}C(O)SR+HX}}}
Нитрозирование тиолов азотистой кислотой или нитрозилхлоридом ведёт к неустойчивым окрашенным нитрозилтиолам (тионитритам):
-
- RSH+HNO2→RSNO+H2O{\displaystyle {\mathsf {RSH+HNO_{2}\rightarrow RSNO+H_{2}O}}}
Эта реакция используется как качественная реакция на тиолы.
Присоединение
Тиолы вступают в реакции присоединения к ацетиленовым, этиленовым и алленовым углеводородам. Реакция может протекать по нуклеофильному, электрофильному либо радикальному механизму.
Окисление
Тиолы окисляются самым широким спектром окислителей (кислород, пероксиды, оксиды азота, галогены и др.). Мягкие окислители (йод, алифатические сульфоксиды, активированный диоксид марганца и т. п.) реагируют с тиолами с образованием дисульфидов:
-
- 2RSH→ORSSR{\displaystyle {\mathsf {2RSH{\xrightarrow{}}RSSR}}}
которые, в свою очередь, при реакции с хлором образуют тиохлориды:
-
- RSSR+Cl2→2RSCl{\displaystyle {\mathsf {RSSR+Cl_{2}\rightarrow 2RSCl}}}
При действии более жёстких окислителей (например, перманганата) сначала образуются сульфиновые кислоты и далее — сульфокислоты:
-
- RSH→ORSO2H→ORSO3H{\displaystyle {\mathsf {RSH{\xrightarrow{}}RSO_{2}H{\xrightarrow{}}RSO_{3}H}}}
В случае окисления тетраацетатом свинца (CH3COO)4Pb в присутствии спиртов окисление идёт с образованием сульфинатов — соответствующих эфиров сульфиновых кислот:
-
- RSH+CH3OH→ORSO2OCH3{\displaystyle {\mathsf {RSH+CH_{3}OH{\xrightarrow{}}RSO_{2}OCH_{3}}}}
В присутствии воды тиолы окисляются хлором до соответствующих сульфонилхлоридов:
-
- RSH→H2O,Cl2RSO2Cl{\displaystyle {\mathsf {RSH{\xrightarrow{H_{2}O,Cl_{2}}}RSO_{2}Cl}}}
Синтез
Алифатические тиолы
Старейшим методом получения тиолов является алкилирование гидросульфидов щелочных металлов с первичными и вторичными алкилгалогенидами, в качестве алкилирующих агентов также могут выступать алкилсульфаты или алкилсульфонаты. Реакция идёт по механизму бимолекулярного нуклеофильного замещения SN2 и проводится обычно в спиртовых растворах, поскольку тиолят-ионы также являются сильными нуклеофилами, побочной реакцией является их дальнейшее алкилирование до сульфидов, снижающее выход тиолов; для повышения выхода необходимо использовать большой избыток гидросульфида:
-
- RX+HS−→RSH+X−{\displaystyle {\mathsf {RX+HS^{-}\rightarrow RSH+X^{-}}}}
-
- RSH+HS−→RS−+H2S{\displaystyle {\mathsf {RSH+HS^{-}\rightarrow RS^{-}+H_{2}S}}}
-
- RS−+RX→R2S+X−; X=Cl, Br, I, ROSO{\displaystyle {\mathsf {RS^{-}+RX\rightarrow R_{2}S+X^{-};\ \ X=Cl,\ Br,\ I,\ ROSO}}}
Более удобным методом синтеза тиолов является алкилирование тиомочевины с образованием алкилтиурониевых солей и их последующим щелочным гидролизом:
Преимуществом этого метода являются легкая очистка перекристаллизацией тиурониевых солей и достаточно высокие общие выходы тиолов.
Своего рода вариацией этого метода, позволяющего получить тиолы без побочного образования сульфидов, является алкилирование с последующим гидролизом ксантогенатов:
-
- C2H5CSSK+RX→C2H5CSSR+KX{\displaystyle {\mathsf {C_{2}H_{5}CSSK+RX\rightarrow C_{2}H_{5}CSSR+KX}}}
-
- C2H5CSSR+H2O→RSH+C2H5OH+CSO{\displaystyle {\mathsf {C_{2}H_{5}CSSR+H_{2}O\rightarrow RSH+C_{2}H_{5}OH+CSO}}}
или тиоацетатов:
-
- CH3COSK+RX→CH3COSR+KX{\displaystyle {\mathsf {CH_{3}COSK+RX\rightarrow CH_{3}COSR+KX}}}
-
- CH3COSR+H2O→RSH+CH3COOH{\displaystyle {\mathsf {CH_{3}COSR+H_{2}O\rightarrow RSH+CH_{3}COOH}}}
Тиолы также могут быть синтезированы из алкилгалогенидов через соли Бунте — соли S-алкилтиосульфокислот, получаемые алкилированием тиосульфата натрия, которые при кислотном гидролизе образуют тиолы:
-
- RX+Na2S2O3→RSSO3Na+NaX{\displaystyle {\mathsf {RX+Na_{2}S_{2}O_{3}\rightarrow RSSO_{3}Na+NaX}}}
-
- RSSO3Na+H2O→RSH+NaHSO4{\displaystyle {\mathsf {RSSO_{3}Na+H_{2}O\rightarrow RSH+NaHSO_{4}}}}
В условиях кислотного катализа сероводород может присоединяться к алкенам с образованием тиолов:
-
- (CH3)2C=CH2+H2S→(CH3)3CSH{\displaystyle {\mathsf {(CH_{3})_{2}C{\text{=}}CH_{2}+H_{2}S\rightarrow (CH_{3})_{3}CSH}}}
Модификацией этого метода является присоединение тиоуксусной кислоты к алкенам с дальнейшим гидролизом образовавшегося алкилтиоацетата:
-
- RCH=CH2+CH3COSH→RCH2CH2SCOCH3{\displaystyle {\mathsf {RCH{\text{=}}CH_{2}+CH_{3}COSH\rightarrow RCH_{2}CH_{2}SCOCH_{3}}}}
-
- RCH2CH2SOCCH3+OH−→RCH2CH2SH+CH3COO−{\displaystyle {\mathsf {RCH_{2}CH_{2}SOCCH_{3}+OH^{-}\rightarrow RCH_{2}CH_{2}SH+CH_{3}COO^{-}}}}
Ароматические тиолы
Ароматические тиолы могут быть синтезированы восстановлением производных ароматических сульфокислот, так, например, тиофенол синтезируется восстановлением бензолсульфохлорида цинком в кислой среде:
-
- C6H5SO2Cl→HC6H5SH{\displaystyle {\mathsf {C_{6}H_{5}SO_{2}Cl{\xrightarrow{}}C_{6}H_{5}SH}}}
Ароматические тиолы также могут быть синтезированы взаимодействием арилдиазониевых солей с гидросульфидами:
-
- ArN2X→HS−ArSH{\displaystyle {\mathsf {ArN_{2}X{\xrightarrow{HS^{-}}}ArSH}}}
или ксантогенатами:
-
- ArN2X→ROC(=S)S−ROC(=S)SAr{\displaystyle {\mathsf {ArN_{2}X{\xrightarrow{ROC({\text{=}}S)S^{-}}}ROC({\text{=}}S)SAr}}}
- ROC(=S)SAr→H2OArSH+ROH+COS{\displaystyle {\mathsf {ROC({\text{=}}S)SAr{\xrightarrow{H_{2}O}}ArSH+ROH+COS}}}
Общие методы
Общим методом синтеза алифатических и ароматических тиолов является взаимодействие реактивов Гриньяра с серой:
-
- RMgX+S→RSMgX{\displaystyle {\mathsf {RMgX+S\rightarrow RSMgX}}}
- RSMgX+H2O→RSH+Mg(OH)X{\displaystyle {\mathsf {RSMgX+H_{2}O\rightarrow RSH+Mg(OH)X}}}
Новости партнеров
«);
obj.attr(‘id’, objId);
obj.addClass(‘news-grid clearfix’);
var objRec = false;
for(i in data) {
var rec = data;
objRec = $(«»);
if(rec)
objRec.addClass(‘news-grid__elem news-grid__elem_ad’);
else
objRec.addClass(‘news-grid__elem’);
objRec.html(»+rec+»);
obj.append(objRec);
}
underNewsEl.append(obj);
$(«#»+objId).find(«a»).click(function(){
var rec_id = $(this).attr(«rec_id»);
var s = document.createElement( ‘img’ );
s.setAttribute( ‘src’, ‘https://relap.io/api/v2/pixel.gif?rid=’+rec_id );
document.body.appendChild( s );
});
}
};
var startContentInsight = function(data) {
if (typeof _ain == ‘undefined’)
return;
if (typeof _ain.track == ‘undefined’)
return;
if (!data) {
data = {};
var el = $(«.newsContent»);
if (el.length) {
data = el.attr(«data-id»);
data = el.attr(«data-url»);
data = el.attr(«data-title»);
data = el.attr(«data-author»);
data = el.attr(«data-section»);
data = el.attr(«data-tags»);
data = el.attr(«data-pubdate»);
}
}
var mainContentId = ‘#newsContent_’ + data + ‘ .news-piece-layout__main’ ;
_ain.id = «1735»;
_ain.url = data;
_ain.postid = data;
_ain.maincontent = mainContentId;
_ain.title = data;
_ain.pubdate = data;
_ain.authors = data;
_ain.sections = data;
_ain.tags = data;
_ain.comments = «»;
_ain.track();
}
Этилмеркаптан
Этилмеркаптан — легколетучая жидкость, обладает сильным неприятным запахом, токсичен, действует на центральную нервную систему, вызывая судороги, паралич и смерть. Даже в ничтожных концентрациях его пары рефлекторно вызывают тошноту, головную боль из-за отвратительного запаха. Одним из продуктов его сгорания является сернистый газ, который не только ядовит, но и коррозионно активен
При одоризации газа персонал одоризационных установок должен быть тщательно проинструктирован и должен соблюдать особые меры предосторожности при работе с ним. Переливать жидкий этилмеркаптан необходимо закрытым способом.
Этилмеркаптан частично растворим в воде, хорошо растворим в спирте, эфире, бензоле, нефти и газовом конденсате. Этилмеркаптан хранится в герметично закрытых бочках в специальных складских помещениях или под навесом вне воздействия солнечных лучей.
Этилмеркаптан взаимодействует с железом и его окислами, образуя склонные к самовозгоранию меркаптиды железа. Установлены факты самовоспламенения пирофорных отложений при — 20 С. Эти отложения состоят в основном из сернистого железа. Медленное воздействие кислорода на пирофорные отложения приводит к постепенному их окислению с выделением элементарной серы, заполняющей поры и покрывающей отложения защитной пленкой.
Этилмеркаптан и более высокомолекулярные гомологи — жидкости, нерастворимые в воде.
Этилмеркаптан производят путем синтеза из этилового спирта и сероводорода: Ш8 С2ШОН — CiHsSH ШО.
Этилмеркаптан свинца, Pb ( SC2Hs) 2 — желтое соединение, плавящееся при 150 и растворимое в хлороформе и бензоле.
Определение этилмеркаптана и образовавшегося из диметил-дисульфида метилмеркаптана производят следующим образом. Из первого поглотительного прибора отбирают для анализа 1 и 5 мл, а из второго — полный объем пробы, доводят недостающий объем до 5 мл раствором ацетата ртути, вносят по 0 5 мл составного реактива и перемешивают.
Производство этилмеркаптанов из хлористого этила было проведено в широком масштабе. Этилмеркаптан применяется в качестве исходного продукта при синтезе сульфонала, весьма распространенного снотворного средства.
Запах этилмеркаптана ощущается при содержании 0 19 г ( 0 22 мл) в 1000 м3 воздуха. Расход жидкого одоранта следует принимать из расчета 1 л на 500 — 20 000 м3 воздуха или инертного газа.
Концентрация этилмеркаптана должна составлять 16 г на 1000 м3 природного газа.
Десорбция этилмеркаптана производится отдув ко и паром при кипячении ( аналогично процессу регенерации моноэтаноламина, см. главу IV) или каким-либо газом при нагревании. Регенерация может проводиться в насадочных аппаратах, однако керамические кольца не выдерживают условий процесса и быстро разрушаются.
Расход этилмеркаптана для одоризации топливного и пускового газа в среднем равен 16 г на 1000 м3 газа.
Поведение этилмеркаптана отлично от поведения высших тиолов. Так, при встряхивании этилмеркаптана с эквимолекулярным количеством ацетата ртути получается неполный меркаптид состава C2H5SHgCl вместо полного меркаптида R — S — Hg — S — R, образующегося в случае других меркаптанов. Формула и температура плавления совпадают с литературными данными. При реакции этилмеркаптана с большим избытком насыщенного раствора сулемы получается комплекс неполного меркацтида ртути С2Н5 — S — HgCl HgCh, что соответствует данным других авторов.
|
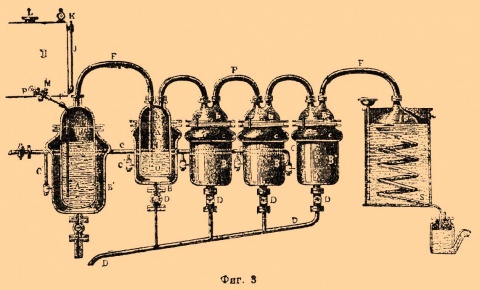
Синтез этилмеркаптана реакцией ацетилена с сероводородом при атмосферном давлении в среде ГМФТА.| Периодический синтез ДВС из ацетилена и сероводорода в 5-литровом реакторе. |
Вынос этилмеркаптана в ловушку наблюдается только после полного превращения щелочи в гидросульфид щелочного металла, что доказано потенциометрическим титрование. По-видимому, здесь реализуется схема , представленная выше. Вероятно, этим и объясняется в данном случае его специфически ускоряющее воздействие на окислительно-восстановительные процессы.
definition — ЭТАНТИОЛ
of Wikipedia
Advertizing ▼
Wikipedia
Этантиол
Материал из Википедии — свободной энциклопедии
Перейти к: ,
| Этантиол | |
| Ethanethiol.svg | |
| Ethanethiol-3D-balls.png | |
| Общие | |
|---|---|
| Химическая формула | С2H6S |
| Молярная масса | 62,1 г/моль |
| Физические свойства | |
| Состояние () | твёрдое/жидкость/газ |
| Плотность | 0,8617 г/см³ |
| Примеси | типичное кол-во |
| Термические свойства | |
| Температура плавления | -148 °C |
| Температура кипения | 35 °C |
| Классификация | |
| Рег. номер CAS | 75-08-1 |
| SMILES | CCS |
Этантиол, этилмеркаптан — органическое соединение, используемое как одорант для природного газа,сжиженного газа. Это летучий тиол, который находится в природе, как компонент нефти. Он малорастворим в воде, но хорошо растворим в большинстве органических растворителей. Был открыт доктором Максвеллом Буроу.
Это бесцветная жидкость с очень сильным отвратительным запахом, напоминающим запах тухлых яиц. Люди могут чувствовать запах этантиола при концентрациях одна часть на 50 миллионов частей воздуха.
Применение
Он добавляется в малых количествах (16 грамм на 1000 кубометров) к природному газу и пропану,(40г на тонну сжиженного газа) который используется для приготовления пищи и отопления, чтобы придать обычно не имеющим запаха газам легко распознаваемый запах, служащий предупреждением об опасной утечке газа. Этантиол также используется как начальное или промежуточное звено при производстве различных видов пластиков, инсектицидов и антиоксидантов.
Действие на организм
Этантиол токсичен, числится в списке сильнодействующих ядовитых веществ и в больших количествах может вызывать головную боль, тошноту и потерю координации, также он поражает почки и печень. Однако дозы полученные от вдыхания одорированного газа далеки от опасных.
| Это незавершённая статья об органическом соединении. Вы можете помочь проекту, исправив и дополнив её. |