Фосфора галогениды
Содержание:
Текст
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ Х. Т. Раудсепп и Э. К. Пийроя СПОСОБ ПОЛУЧЕНИЯ ХЛОРОКИСИ ФОСФОРАЗаилео 9 аггуста 1987 г. за Са 88788 а Комитет ио делам зобретеиий открытий ири Совете Мииистрои СССРИзвестен спосоо получения хлор- окиси фосфора, являюцейся важным промежуточным продуктом при получении сложных эфиров фосфорной кислоты, путем окисления треххлористого фосфора кислородом в пр, — сутствии катализатора — ортофоссадорно кислоты при небольшом давлении, а также в присутствии катализатора — соединения марганца в виде ацетоювого раствора пермангзнзтз каля, смешиваемого с трех- хлористым фосфором и пропусканил в полученную смесь гззообразнокислорода с дистилляцией полсчсниого продукта,Предлагается способ получения хлорокиси фосфора, согласно кото. рому окисление трехх;орстого фосфора кислородом при нормально.дзвлеши осуцествляется путем пропускапия смеси паров треххлористого фосфора с кислородом над поверхностью нагретого до 350 — 550 катализатора, в качестве которого применяются окись ванадия или окислы хрома, молиодена, вольфрама, железа, осия, меди, серебра или марганца в чистом виле или в виде нансссниых нз поверхность инертных ностолей,Г 1 рсдла гаем ый способ обеспечивает увеличение выхода хлорокиси фосфора, по сравненшо с извсстьы способом.П р и м е р 1. ь 1 срсз кварцевую трубку, нагретую до температуры 400 — 425 изполнен о еусочзми фарфора, поверхность которого покрыта окисью ванадия, пропускают парь треххлористого фосфора с техническим кислородом при молярнсм соотношснии кислорода к тре.»- хлористому фосфору 0,75: 1,0. Получешую пзрогззовую смесь охлаждают в холодильнике. Выход образовавшейся хлорокиси фосфора — 85;1 от теоретического. По данным анализа, онз не содержит треххлористо, о сросфорз.Прим ер 2. Смесь ислородз и треххлористого фосфора взятых и молярньх соотношениях 1: 1) пропускают над нагретым катализатором. Катализатором являются кусочк 1 глины диаметром 2 — 3 хн, пропитанные раствором ьзнздата амхошя и прокаленные при температуре 450 — 550. Температуру в рсзкцион.112079 дом в присутствии катализатора, о тлич аюгцийся тем, что, с целью Предмет изобретения Способ получения хлорокиси фосфора путем окисления треххлорнстого фосфора газообразным кислороОтв. редактор Л. П. Ситников Стандартгиз. Подп. к печ. 16/% 1958 г. Объем 0,125 и. л. Тираж 380. Цена 25 кон,1 ппографня Комитета по делам изобретений и открытий при Совете Министров СССР Москва, Неглинная, д. 23, Зак. 1891ной зоне трубки, наполненной катализатором, поддерживают в пределах 450 в 5. Окисление треххлорнстого фосфора протекает быстро.Полученная охлаждением парогазовой смеси хлорокись фосфора не содержит треххлористого фосфора. Выход хлорокиси фосфора — 8 б% от теоретического. увеличения выходов продукта, смесь паров треххлористого фосфора с кп. слородом пропускают над нагретой до 350 в 5 поверхностью катализатора, в качестве которого приме. няют окись ванадия или окислы хрома, молибдена, вольфрама, железа, меди, осмия, серебра или марганца в чистом виде или в виде нанесенных на поверхность инертных носителей.
Смотреть
Получение
Действие хлористого водорода на оксид фосфора:
-
- P4O10+3HCl →200oC POCl3+3HPO3{\displaystyle {\mathsf {P_{4}O_{10}+3HCl\ {\xrightarrow {200^{o}C}}\ POCl_{3}+3HPO_{3}}}}
Действие хлорида фосфора на оксид фосфора:
-
- P4O10+6PCl5 →150−175oC 10POCl3{\displaystyle {\mathsf {P_{4}O_{10}+6PCl_{5}\ {\xrightarrow {150-175^{o}C}}\ 10POCl_{3}}}}
Окисление кислородом трихлорида фосфора:
-
- 2PCl3+O2 →50−60oC 2POCl3{\displaystyle {\mathsf {2PCl_{3}+O_{2}\ {\xrightarrow {50-60^{o}C}}\ 2POCl_{3}}}}
Разложение пентахлорида фосфора:
-
- PCl5+SO2 →50−60oC POCl3+SCl2O{\displaystyle {\mathsf {PCl_{5}+SO_{2}\ {\xrightarrow {50-60^{o}C}}\ POCl_{3}+SCl_{2}O}}}
- 2PCl5+CaSO3 →50−60oC 2POCl3+SCl2O+CaCl2{\displaystyle {\mathsf {2PCl_{5}+CaSO_{3}\ {\xrightarrow {50-60^{o}C}}\ 2POCl_{3}+SCl_{2}O+CaCl_{2}}}}
- PCl5+H2SO4 → POCl3+HCl+HSO3Cl{\displaystyle {\mathsf {PCl_{5}+H_{2}SO_{4}\ {\xrightarrow {}}\ POCl_{3}+HCl+HSO_{3}Cl}}}
- 3PCl5+2B(OH)3 →150oC 3POCl3+6HCl+B2O3{\displaystyle {\mathsf {3PCl_{5}+2B(OH)_{3}\ {\xrightarrow {150^{o}C}}\ 3POCl_{3}+6HCl+B_{2}O_{3}}}}
Химические свойства
Тиофен принадлежит к π-избыточным гетероароматическим системам и проявляет ароматические свойства. Вступает в реакции электрофильного замещения, в частности, реакции галогенирования, нитрования, формилирования, и др., причём его активность в этих реакциях выражена значительно сильнее, чем бензола — для некоторых реакций на 4 порядка. Данные реакции как правило направлены в α-положение цикла, а в β-положение — на 2—3 порядка медленнее. Производные тиофена, которые в положении 2 имеют ориентанты II рода, вступают в реакции замещения с образованием 2,5-дизамещенных. 2,4-Изомеры синтезируют при использовании исходных реагентов в виде комплексов с сильными протонными или апротонными кислотами: это обусловлено значительным возрастанием электроноакцепторной способности заместителя вследствие комплексообразования:

Тиофен и его производные менее стабильны, чем их бензольные аналоги, поэтому многие реакции в ряду тиофена сопровождаются поликонденсацией (смолообразованием) и деструкцией. Тиофен достаточно гладко алкилируется лишь в мягких условиях при использовании более активных третичных и вторичных (но не первичных) алкилгалогенидов. Тиофен и его замещенные, содержащие ориентанты I рода, очень легко ацилируются в присутствии SnCl4 или SnCl2 в бензоле, который в этих условиях не ацилируется. Формилирование тиофена протекает под действием ДМФА или N-метилформанилида в присутствии POCl3; взаимодействует с альдегидами и кетонами в присутствии апротонных или протонных кислот приводит к образованию соединений ряда ди(2-тиенил)метана.
Тиофен и его производные способны к прямому металлированию под действием литийорганических соединений по механизму так называемого протофильного замещения. Реакция протекает быстро и практически количественно при комнатной температуре в большинстве случаев с высокой региоспецифичностью с образованием α-металлированных производных. В очень мягких условиях (-70 °C) под действием C4H9Li протекает также реакция обмена атома галогена в цикле тиофена на металл, причем обмен галогена в α-положении предпочтительнее, чем в β-положении, а обмен I на Li идет легче, чем Br. В реакции нуклеофильного замещения легко вступают главным образом замещенные тиофена, содержащие в цикле ориентанты II рода.
Тиофен его гомологи и некоторые производные способны к реакциям радикального замещения, например арилированию по реакции Гомберга-Бахмана-Хея. Др. важнейший способ арилирования-УФ облучение иодтиофена в ароматическом растворителе или иодпроизводного ароматического характера в тиофене.
Свойства непредельных соединений выражены в тиофене слабо. Так, в диеновый синтез вступают только конденсированные тиофены, например, замещенные бензотиофена. Гидрирование в ряду тиофена идет обычно с трудом, что связано с его отравляющим действием на многие катализаторы. Тем не менее тиофен в присут. Pd/C, MoS2, и др. превращается в тетрагидротиофен (тиофан, температура плавления −96,2 °C, температура кипения 121,1 °C, 4° d204 0,9987, n20D 1,54048). Гомологи тиофена и многие замещенные легко превращаются в соответствующие производные тиофана в условиях ионного гидрирования, например при действии трифторуксусной кислоты и триэтилсилана. Дигидротиофен образуется при восстановлении тиофена Na в жидком NH3. При аналогичном восстановлении гомологов тиофена и его производных процесс обычно не останавливается на стадии образования дигидропроизводных, а происходит расщепление цикла с образованием соответствующих соединений алифатического ряда, например:

При действии скелетного Ni с участием адсорбированного Н, идет восстановительная десульфуризация замещенных тиофена с образованием алифатических соединений:

Эта реакция — один из путей получения из производных тиофена соединения различных классов, например карбоновых кислот, высших спиртов, простых эфиров, аминоспиртов и аминокислот, а также лактамов макроциклических кетонов, кетокислот и кетолактонов.
Тиофен и его замещенные сравнительно устойчивы к действию окислителей. Однако при действии Н2О2 или надкислот происходит окисление до сульфоксида (в свободном состоянии не выделен) или до сульфона. Оба эти соединения представляют собой типичную диеновую систему, способную, например, к диеновому синтезу, в котором они могут выполнять роль как диена, так и диенофила.
Под действием некоторых алкилирующих агентов или ди-(этоксикарбонил) карбена образуются производные тиофена с положительно заряженным трехвалентным (сульфониевым) атомом серы, например:
Источники и способы получения
Тиофен и его гомологи содержатся в продуктах коксования каменного угля (откуда их и выделяют вместе с каменноугольным бензолом) и продуктах термического разложения сланцев (в некоторых фракциях до 70 % по массе). В сыром бензоле содержание тиофена составляет 1,3—1,4 %, в получаемом из сырого бензола тиофено-бензольном концентрате-30—35 %. Основное сырье для синтеза тиофена и его гомологов — углеводороды нефтяных фракций С4 и С5, из которых они могут быть получены термическим взаимодействием с S или каталитической реакцией с H2S или SO2. Тиофен синтезируют также пропусканием фурана, ацетилена или 1,3-бутадиена и H2S над Al2O3. Гомологи тиофена, а также некоторые производные — получают замыканием соответствующих 1,4-дикарбонильных соединений с помощью P2S5, например:

Оксихлорид — фосфор
Оксихлорид фосфора РОС13 образуется из РС15 также при его взаимодействии с веществами, содержащими ОН-группы, например с органическими кислотами, превращая их в хлорангидриды.
Оксихлорид фосфора является хлорангидридом фосфорной кислоты и при гидролизе превращается в эту кислоту.
Оксихлорид фосфора РОС13 — бесцветная, сильно преломляющая свет, дымящая во влажном воздухе жидкость; удельный вес 1 72, температура кипения 108 7, температура плавления 1 3; в чистом виде удобнее всего получается при действии пятихлористого фосфора на щавелевую кислоту РС1Б Н2С204 РОС13 2НС1 С02 СО.
Оксихлорид фосфора РОС13 — бесцветная, сильно преломляющая свет, дымящая во влажном воздухе жидкость; удельный вес 1 72, температура кипения 108 7, температура плавления 1 3; в чистом виде удобнее всего получается при действии пятихлористого фосфора на щавелевую кислоту Ш5 Н2С204РОС13 2НС14 — С02 СО.
Оксихлорид фосфора РОС13 — бесцветная, сильно преломляющая свет, дымящая во влажном воздухе жидкость; удельный вес 1 72, температура кипения 108 7, температура плавления 1 3; в чистом виде удобнее всего получается при действии пятихлористого фосфора на щавелевую кислоту РС15 Н2С2О4РОС13 2НС1 С02 СО.
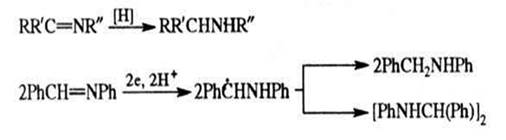
Оксихлорид фосфора также взаимодействует с N-алкилами-дами; продуктами реакции обычно являются соответствующие нитрилы ср
Важное различие состоит в том, что алкилгалогенид обычно не является вторым продуктом, и в том, что R2 реагирует с ароматическим растворителем или теряет протон, давая олефин; однако причины такого различия пока не ясны. Интермедиатом в данной реакции почти наверняка является соединение, аналогичное комплексу Вильсмейера ( 144), однако внутримолекулярный отрыв протона фосфорильным или сульфонильным кислородом приводит к образованию изоцианида.
Оксихлорид фосфора обладаем раздражающим действием.
Оксихлорид фосфора реагирует со многими веществами, например водой.
С оксихлоридами фосфора и серы, РОС13 и SO2C12, хлорная кислота смешивается без заметного взаимодействия.
В оксихлориде фосфора , тионилхлориде и ацетилхлориде были исследованы сульфон-фталеиновые индикаторы. Изменения окраски, обратимо осуществляющиеся при определенных значениях рсь не зависят ни от природы растворителя, ни от природы растворенного вещества, изменяющего активность иона хлора в растворе. В среде с высокой активностью иона хлора растворы имеют слабую желтую окраску, а в среде с низкой активностью иона хлора — красную.
Механизм действия оксихлорида фосфора и аналогичных растворителей было предложено описывать таким же образом ; однако, по-видимому, решающим фактором, который следует учитывать, является взаимодействие между растворителем и растворенным веществом. Было найдено, что пента-хлорид сурьмы и хлорид алюминия очень медленно обмениваются с оксихлоридом фосфора, используемым в качестве растворителя при с — 10 — 2 М, но в присутствии ионов хлора обмен происходит быстрее.
Таким образом, очищенный оксихлорид фосфора содержит приблизительно 10 — 4 моля воды в 1 л и это нужно принимать во внимание при рассмотрении чистого растворителя или разбавленных растворов.
Хлористый сульфурил S02C12, оксихлорид фосфора РОС13, а также растворы двуокиси серы SO2 в органических растворителях, входящих в состав неводных электролитов, восстанавливаются на углеродном электроде аналогично хлористому тионилу.
Метод основан на определении оксихлорида фосфора по синему фосфорно-молибденовому комплексу.
К ним относятся хлориды и оксихлориды фосфора, титана, ванадия, бора, олова и сурьмы. Растворы таких компонентов в SiCl4 по свойствам приближаются к регулярным растворам, относительная летучесть этих растворов может быть с достаточной точностью рассчитана по уравнению Гильденбранда — Вуда. Примеси соединений кальция, магния, железа, алюминия, марганца, свинца и других дают квазиазеотропные смеси с SiCl4 и ректификацией практически не отделяются.
Chemical properties
POCl3 reacts with water to give hydrogen chloride and phosphoric acid:
- O=PCl3 + 3 H2O → O=P(OH)3 + 3 HCl
Intermediates in the conversion have been isolated, including pyrophosphoryl chloride, P2O3Cl4.
Upon treatment with excess alcohols and phenols, POCl3 gives phosphate esters:
- O=PCl3 + 3 ROH → O=P(OR)3 + 3 HCl
Such reactions are often performed in the presence of an HCl acceptor such as pyridine or an amine.
POCl3 can also act as a Lewis base, forming adducts with a variety of Lewis acids such as titanium tetrachloride:
- Cl3PO + TiCl4 → Cl3POTiCl4
The aluminium chloride adduct (POCl3·AlCl3) is quite stable, and so POCl3 can be used to remove AlCl3 from reaction mixtures, for example at the end of a Friedel-Crafts reaction.
POCl3 reacts with hydrogen bromide in the presence of Lewis-acidic catalysts to produce POBr3.
Глава 13. Упражнения повышенной сложности
1. Два изомерных мононитропроизводных C5H6N2O2 образуются в соотношении 6:1 при взаимодействии 2-метилпиррола с Ac2O/HNO3. Каково строение основного продукта реакции?
2. Приведите структурные формулы соединений образующихся в результате следующих реакций: а) при взаимодействии пиррола с Cl3CCOCl, затем полученного соединения с Br2 и затем продукта реакции с MeONa/MeOH → C6H6BrNO2; б) при взаимодействии пиррола с диметилформамидом /POCl3, затем продукта реакции с MeCOCl/AlCl3 и на заключительной стадии с водным NaOH → C7H7NO2, в) при реакции 2-хлорпиррола с диметилфорамидом/POCl3, затем водным NaOH и затем продукта реакции с LiAlH4 → C5H6ClN.

3. Приведите структурные формулы соединений, образующихся на конечной стадии в каждом случае при реакции пиррола с POCl3 иа) N,N-диметилбензамидом;б) N,N-диметиламидом пиррол-2-карбоновой кислоты;в) 2-пирролидоном и водным раствором гидроксида натрия.

4. При обработке 2-метилпиррола HCl образуется димер, а не тример, как в случае самого пиррола (разд. 13.1.8). Предложите структурную формулу димера C10H14N2 и объясните, почему в этом случае не образуется тримера.

5. При взаимодействии 2,5-диметилпиррола с Zn/HCl образуется смесь двух изомерных продуктов реакции C6H11N. Предложите их структурные формулы.
6. а) При нагревании 1-метоксикарбонилпиррола с диэтиловым эфиром ацетилен-дикарбоновой кислоты при 160 °C образуется диэтиловый эфир 1-метоксикарбонилпиррол-3,4-дикарбоновой кислоты. Предложите механизм процесса и структуры образующихся интермедиатов,б) Предложите структурную формулу соединения C11H12N2O2, образующегося при последовательном взаимодействии 1-метоксикарбонилпиррола с синглетным кислородом и затем со смесью 1-метилпиррола и SnCl2.

7. Предложите структурные формулы соединений, образующихся на каждой стадии при взаимодействии пиррола последовательно со следующими реагентами:a) Me2NH/HCHO/AcOH; б) CH3I; в) пиперидин в горячем этаноле → C10H16N2.

8. Предложите способы получения а) 1-пропилпиррола; б) 1 -(тиен-2-ил)пиррола;в) 1-фенилсульфонилпиррола из соединений, не содержащих пиррольный цикл.

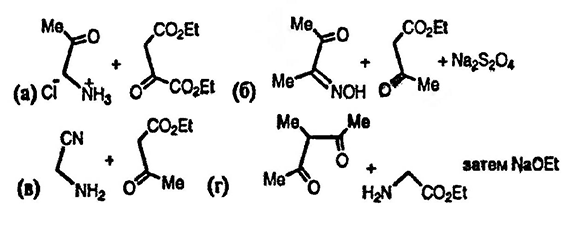
9. Взаимодействие этилового эфира ацетоуксусной кислоты с HNO2 и затем с Zn/AcOH и впоследствии с пентан-2,4-дионом приводит к образованию пиррола C11H15NO3. Предложите структурную формулу пиррола, последовательность приводящую к его образованию, и способ его превращения в 2,4-диметил-3-этилпиррол.

10. Предложите способы получения следующих соединений: а) диэтилового эфира 4-метилпиррол-2,3-дикарбоновой кислоты; б) этилового эфира 2,4,5-триметил-пиррол-3-карбоновой кислоты; в) этилового эфира 4-амино-2-метилпиррол-3-карбоновой кислоты; г) этилового эфира 3,4,5-триметилпиррол-2-карбоновой кислоты.
Preparation
Phosphoryl chloride can be prepared by many methods. Phosphoryl chloride was first reported in 1847 by the French chemist Adolphe Wurtz by reacting phosphorus pentachloride with water.
By oxidation
The commercial method involves oxidation of phosphorus trichloride with oxygen:
- 2 PCl3 + O2 → 2 POCl3
An alternative method involves the oxidation of phosphorus trichloride with potassium chlorate:
- 3 PCl3 + KClO3 → 3 POCl3 + KCl
Oxygenations
The reaction of phosphorus pentachloride (PCl5) with phosphorus pentoxide (P4O10).
-
- 6 PCl5 + P4O10 → 10 POCl3
The reaction can be simplified by chlorinating a mixture of PCl3 and P4O10, generating the PCl5in situ.
The reaction of phosphorus pentachloride with boric acid or oxalic acid:
- 3 PCl5 + 2 B(OH)3 → 3 POCl3 + B2O3 + 6 HCl
- PCl5 + (COOH)2 → POCl3 + CO + CO2 + 2 HCl
Other methods
Reduction of tricalcium phosphate with carbon in the presence of chlorine gas:
- Ca3(PO4)2 + 6 C + 6 Cl2 → 3 CaCl2 + 6 CO + 2 POCl3
The reaction of phosphorus pentoxide with sodium chloride is also reported:
- 2 P2O5 + 3 NaCl → 3 NaPO3 + POCl3.
Свойства
При нагревании выше 300 °C полностью разлагается на PCl3 и Cl2.
Пентахлорид фосфора типичное кислотное соединение. Он энергично реагирует с водой, образуя по первой стадии оксохлорид фосфора (V):
В горячей воде гидролиз протекает полностью, до образования ортофосфорной кислоты:
Для РCl5 характерны реакции окислительного хлорирования:
C концентрированной серной кислотой образует хлорсульфоновую кислоту:
При нагревании РCl5 и NH4Cl происходит реакция образования полимера фосфонитрилхлорида:
(PNCl2)n — прозрачное эластичное вещество, «неорганический каучук». Выдерживает нагревание выше 200 °C. Однако фосфонитрилхлорид сравнительно легко гидролизуется, что затрудняет его практическое использование. Заменой атомов хлора на органические радикалы можно получить водоустойчивые полимеры.
Uses
In one commercial application, phosphoryl chloride is used in the manufacture of phosphate esters. Triarylphosphates such as triphenyl phosphate and tricresyl phosphate are used as flame retardants and plasticisers for PVC. Trialkylphosphates such as tributyl phosphate are used as liquid–liquid extraction solvents in nuclear reprocessing and elsewhere.
In the semiconductor industry, POCl3 is used as a safe liquid phosphorus source in diffusion processes. The phosphorus acts as a dopant used to create n-type layers on a silicon wafer.[citation needed]
As a reagent
In the laboratory, POCl3 is a reagent in dehydrations. One example involves conversion of primary amides to nitriles:
- RC(O)NH2 + POCl3 → RCN + «PO2Cl» + 2 HCl
In a related reaction, certain aryl-substituted amides can be cyclised using the Bischler-Napieralski reaction.
Such reactions are believed to proceed via an imidoyl chloride. In certain cases, the imidoyl chloride is the final product. For example, pyridones and pyrimidones can be converted to chloro- derivatives such as 2-chloropyridines and 2-chloropyrimidines, which are intermediates in the pharmaceutical industry.
In the Vilsmeier-Haack reaction, POCl3 reacts with amides to produce a «Vilsmeier reagent», a chloro-iminium salt, which subsequently reacts with electron-rich aromatic compounds to produce aromatic aldehydes upon aqueous work-up.
Химические свойства
Фосфор в PCl3 находится в степени окисления +3, а хлор — в степени −1. Многие из свойств соединения обусловлены именно этими обстоятельствами. В присутствии воды — дымит и разлагается.
PCl3 — базовый продукт для других производных фосфора, получаемых из него при окислении до пентахлорида(PCl5), тиофосфорилхлорида (PSCl3) или оксихлорида (POCl3).
Если пропустить электрический разряд через смесь пара PCl3 и газообразного водорода, образуется редкий сложный хлорид фосфора с формулой P2Cl4.
Известно большое число сходных реакций замещения, в том числе и с органическими веществами — спиртами и фенолами:
Спирты реагируют сходным образом:
Наличие неподелённой электронной пары у атомов фосфора обуславливает способность трихлорида проявлять донорные свойства, образуя электронейтральные комплексы, например, [Ni(PCl3)4] По химической природе трихлорид фосфора является хлорангидридом фосфористой кислоты. Гидролиз её приводит к образованию двух кислот, а взаимодействие со щелочами — двух солей: